Алкены — Гипермаркет знаний. Алкены
В органической химии можно встретить углеводородные вещества с разным количеством углерода в цепи и C=C-связью. Они являются гомологами и называются алкенами. Из-за своего строения они химически более активны, чем алканы. Но какие именно реакции для них характерны? Рассмотрим их распространение в природе, разные способы получения и применение.
Что из себя представляют?
Алкены, которые также называются олефинами (маслянистые) получили свое название от этен-хлорида, производного первого представителя этой группы. У всех алкенов есть хотя бы одна двойная C=C-связь. C n H 2n - формула всех олефинов, а название образовывается от алкана с таким же количеством углеродов в молекуле, только суффикс -ан меняется на -ен. Арабской цифрой в конце названия через дефис обозначают номер углерода, от которого начинается двойная связь. Рассмотрим основные алкены, таблица поможет вам запомнить их:
Если молекулы имеют простое неразветвленное строение, то добавляют суффикс -илен, это также отражено в таблице.
Где их можно встретить?
Так как реакционная способность алкенов весьма высока, их представители в природе встречаются крайне редко. Принцип жизни молекулы олефинов — "давай дружить". Нет вокруг других веществ — не беда, будем дружить между собой, образуя полимеры.
Но они есть, и небольшое количество представителей входит в состав сопутствующего нефтяного газа, а высших — в нефти, добываемой на территории Канады.
Самый первый представитель алкенов этен — это гормон, стимулирующий созревание плодов, поэтому его в небольших количествах синтезируют представители флоры. Есть алкен цис-9-трикозен, который у самок мухи домашней играет роль полового аттрактанта. Еще его называют мускалур. (Аттрактант — вещества природного или синтетического происхождения, которое вызывает влечение к источнику запаха у другого организма). С точки зрения химии, алкен этот выглядит так:
Так как весьма ценным сырьем являются все алкены, способы получения их искусственным путем весьма разнообразны. Рассмотрим наиболее распространенные.
А если нужно много?
В промышленности класс алкенов, в основном, получается при крекинге, т.е. расщеплении молекулы под воздействием высоких температур, высших алканов. Для реакции необходим нагрев в диапазоне от 400 до 700 °C. Расщепляется алкан так, как ему захочется, образуя алкены, способы получения которых мы рассматриваем, с большим количеством вариантов строения молекул:
C 7 H 16 -> CH 3 -CH=CH 2 + C 4 H 10.
Еще один распространенный способ называется дегидрирование, при котором от представителя ряда алкана в присутствии катализатора отделяют молекулу водорода.
В лабораторных условиях алкены и способы получения отличаются, они основаны на реакциях элиминирования (отщепления группы атомов без их замещения). Чаще всего элиминируются атомы воды из спиртов, галогены, водород или галогенводород. Наиболее распространенный способ получения алкенов — из спиртов в присутствии кислоты, как катализатора. Возможно использование и других катализаторов
Все реакции элиминирования подчинены правилу Зайцева, гласящему:
Атом водорода отщепляется от того углерода, соседствующего с углеродом, несущим группу -OH, у которого меньше водородов.

Применив правило, ответьте, какой продукт реакции будет преобладать? Позже вы узнаете, правильно ли ответили.
Химические свойства
Алкены активно реагируют с веществами, разрывая свою пи-связь (еще одно название связи C=C). Ведь она не такая прочная, как одинарная (сигма-связь). Углеводород из ненасыщенного превращается в насыщенный, не образуя других веществ после реакции (присоединение).
- присоединение водорода (гидрирование). Присутствие катализатора и нагревания нужна для ее прохождения;
- присоединение молекул галогенов (галогенирование). Является одной из качественных реакций на пи-связь. Ведь при реакции алкенов с бромной водой, она из бурой становится прозрачной;
- реакция с галогенводородами (гидрогалогенирование);
- присоединение воды (гидратация). Условиями прохождения реакции является нагревание и присутствие катализатора (кислоты);
Реакции несимметричных олефинов с галогенводородами и водой подчиняются правилу Марковникова. А значит, водород присоединится к тому углероду из двойной углерод-углеродной связи, у которого уже больше атомов водорода.

- горение;
- неполное окисление каталитическое. Продуктом являются циклические оксиды;
- реакция Вагнера (окисление перманганатом в нейтральной среде). Эта реакция алкенов — еще одна качественная C=C-связь. При протекании розовый раствор марганцовки обесцвечивается. Если ту же реакцию провести в соединенной кислой среде, продукты будут уже другими (карбоновые кислоты, кетоны, углекислый газ);
- изомеризация. Характерны все виды: цис- и транс-, перемещение двойной связи, циклизация, скелетная изомеризация;
- полимеризация — главное свойство олефинов для промышленности.
Применение в медицине
Большое практическое значение имеют продукты реакции алкенов. Многие из них используются в медицине. Из пропена получают глицерин. Этот многоатомный спирт является прекрасным растворителем, причем, если его использовать вместо воды, растворы будут более концентрированными. В медицинских целях в нем растворяют алкалоиды, тимол, йод, бром и др. Также глицерин применяют при приготовлении мазей, паст и кремов. Он предотвращает их высыхание. Сам по себе глицерин является антисептиком.
При реакции с хлороводородом получаются производные, которые применяются как местная анестезия при нанесении на кожу, а также для кратковременного наркоза при незначительных хирургических вмешательствах, при помощи ингаляций.

Алкадиены — это алкены с двумя двойными связями в одной молекуле. Основное их применение — производство синтетического каучука, из которого потом изготавливают различные грелки и спринцовки, зонды и катетеры, перчатки, соски и многое другое, что просто незаменимо при уходе за больными.
Применение в промышленности
| Вид промышленности | Что применяют | Каким образом могут использовать |
| Сельское хозяйство | этен | ускоряет созревание овощей и фруктов, дефолиация растений, пленки для теплиц |
| Лако-красочная | этен, бутен, пропен и др. | для получения растворителей, эфиров, сольвента |
| Машиностроение | 2-метилпропен, этен | производство синтетического каучука, смазочные масла, антифриз |
| Пищевая промышленность | этен | производство тефлона, этилового спирт, уксусная кислота |
| Химическая промышленность | этен, полипропилен | получают спирты, полимеры (поливинилхлорид, полиэтилен, поливинилацетат, полиизобтилен, уксусный альдегид |
| Горная промышленность | этен и др. | взрывчатые вещества |
Более широкое применение нашли алкены и их производные в промышленности. (Где и как используются алкены, таблица выше).

Это лишь малая часть использования алкенов и их производных. С каждым годом потребность в олефинах только возрастает, а значит, возрастает потребность и в их производстве.
Физические свойства алкенов похожи на свойства алканов, хотя все они имеют несколько более низкие температуры плавления и кипения, чем соответствующие алканы. Например, пентан имеет температуру кипения 36 °С, а пентен-1 - 30 °С. При обычных условиях алкены С 2 — С 4 - газы. С 5 – С 15 - жидкости, начиная с C 16 - твердые вещества. Алкены не растворимы в воде, хорошо растворимы в органических растворителях.
В природе алкены встречаются редко. Поскольку алкены являются ценным сырьем для промышленного органического синтеза, разработаны многие способы их получения.
1. Основным промышленным источником алкенов служит крекинг алканов, входящих в состав нефти:
3. В лабораторных условиях алкены получают по реакциям отщепления (элиминирования), при которых от соседних атомов углерода отщепляются два атома или две группы атомов, и образуется дополнительная p -связь. К таким реакциям относятся следующие.
1) Дегидратация спиртов происходит при их нагревании с водоотнимающими средствами, например с серной кислотой при температуре выше 150 °С:
При отщеплении Н 2 O от спиртов, НВr и HCl от алкилгалогенидов атом водорода преимущественно отщепляется от того из соседних атомов углерода, который связан с наименьшим числом атомов водорода (от наименее гидрогенизированного атома углерода). Эта закономерность носит название правила Зайцева .
3) Дегалогенирование происходит при нагревании дигалогенидов, имеющих атомы галогена у соседних атомов углерода, с активными металлами:
CH 2 Br —CHBr —CH 3 + Mg → СН 2 =СН-СН 3 + Mg Вr 2 .
Химические свойства алкенов определяются наличием в их молекулах двойной связи. Электронная плотность p -связи достаточно подвижна и легко вступает в реакции с электрофильными частицами. Поэтому многие реакции алкенов протекают по механизму электрофильного присоединения , обозначаемому символом A E (от англ, addition electrophilic ). Реакции злектрофильного присоединения это ионные процессы, протекающие в несколько стадий.
На первой стадии электрофильная частица (чаще всего это бывает протон H +) взаимодействует с p -электронами двойной связи и образует p -комплекс, который затем превращается в карбокатион путем образования ковалентной s -связи между электрофильной частицей и одним из атомов углерода:
алкен p -комплекс карбокатион
На второй стадии карбокатион реагирует с анионом X — , образуя вторую s -связь за счет электронной пары аниона:
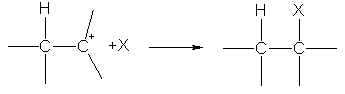
Ион водорода в реакциях электрофильного присоединения присоединяется к тому из атомов углерода при двойной связи, на котором больше отрицательный заряд. Распределение зарядов определяется смещением p
-электронной плотности под влиянием заместителей:  .
.
Электронодонорные заместители, проявляющие +I -эффект, смещают p -электронную плотность к более гидрогенизированному атому углерода и создают на нем частичный отрицательный заряд. Этим объясняется правило Марковникова : при присоединении полярных молекул типа НХ(X = Hal , ОН, CN и т.п.) к несимметричным алкенам водород преимущественно присоединяется к более гидрогенизированному атому углерода при двойной связи.
Рассмотрим конкретные примеры реакций присоединения.
1) Гидрогалогенирование . При взаимодействии алкенов с галогеноводородами (HCl , НВr ) образуются алкилгалогениды:
СН 3 -СН=СН 2 + НВr ® СН 3 -СНВr-СН 3 .
Продукты реакции определяются правилом Марковникова.
Следует, однако, подчеркнуть, что в присутствии какого-либо органического пероксида полярные молекулы НХ реагируют с алкенами не по правилу Марковникова:
| R-O-O-R | ||
| СН 3 -СН=СН 2 + НВr | СН 3 -СН 2 -СН 2 Вr |
Это связано с тем, что присутствие перекиси обусловливает радикальный, а не ионный механизм реакции.
2) Гидратация . При взаимодействии алкенов с водой в присутствии минеральных кислот (серной, фосфорной) образуются спирты. Минеральные кислоты выполняют роль катализаторов и являются источниками протонов. Присоединение воды также идет по правилу Марковникова:
СН 3 -СН=СН 2 + НОН ® СН 3 -СН(ОН)-СН 3 .
3) Галогенирование . Алкены обесцвечивают бромную воду:
СН 2 =СН 2 + Вr 2 ® ВrСН 2 -СН 2 Вr.
Эта реакция является качественной на двойную связь.
4) Гидрирование . Присоединение водорода происходит под действием металлических катализаторов:
где R = Н, СН 3 , Cl , С 6 Н 5 и т.д. Молекула CH 2 =CHR называется мономером, полученное соединение - полимером , число n-степень полимеризации.
Полимеризация различных производных алкенов дает ценные промышленные продукты: полиэтилен, полипропилен, поливинилхлорид и другие.
Кроме присоединения, для алкенов характерны также реакции окисления. При мягком окислении алкенов водным раствором перманганата калия (реакция Вагнера ) образуются двухатомные спирты:
ЗСН 2 =СН 2 + 2КМn О 4 + 4Н 2 О ® ЗНОСН 2 -СН 2 ОН + 2MnO 2 ↓ + 2KOH .
В результате протекания этой реакции фиолетовый раствор перманганата калия быстро обесцвечивается и выпадает коричневый осадок оксида марганца (IV ). Эта реакция, как и реакция обесцвечивания бромной воды, является качественной на двойную связь. При жестком окислении алкенов кипящим раствором перманганата калия в кислой среде происходит полный разрыв двойной связи с образованием кетонов, карбоновых кислот или СО 2 , например:
| [О] | ||
| СН 3 -СН=СН-СН 3 | 2СН 3 -СООН |
По продуктам окисления можно установить положение двойной связи в исходном алкене.
Как и все другие углеводороды, алкены горят, и при обильном доступе воздуха образуют диоксид углерода и воду:
С n Н 2 n + Зn /2О 2 ® n СО 2 + n Н 2 О.
При ограниченном доступе воздуха горение алкенов может приводить к образованию монооксида углерода и воды:
С n Н 2n + nО 2 ® nCO + nH 2 O .
Если смешать алкен с кислородом и пропустить эту смесь над нагретым до 200°С серебряным катализатором, то образуется оксид алкена (эпоксиалкан), например:

При любых температурах алкены окисляются озоном (озон более сильный окислитель, чем кислород). Если газообразный озон пропускают через раствор какого-либо алкена в тетрахлор-метане при температурах ниже комнатной, то происходит реакция присоединения, и образуются соответствующие озониды (циклические перекиси). Озониды очень неустойчивы и могут легко взрываться. Поэтому обычно их не выделяют, а сразу после получения разлагают водой - при этом образуются карбонильные соединения (альдегиды или кетоны), строение которых указывает на строение подвергавшегося озонированию алкена.
Низшие алкены - важные исходные вещества для промышленного органического синтеза. Из этилена получают этиловый спирт, полиэтилен, полистирол. Пропен используют для синтеза полипропилена, фенола, ацетона, глицерина.
Алкены - непредельные углеводороды, в составе которых есть одна двойная связь. Примеры алкенов:

Методы получения алкенов.
1. Крекинг алканов при 400-700°С. Реакция идет по свободнорадикальному механизму:

2. Дегидрирование алканов:
3. Реакция элиминирования (отщепление): от соседних атомов углерода отщепляются 2 атома или 2 группы атомов, и образуется двойная связь. К таким реакциям относят:
А) Дегидратацию спиртов (нагрев свыше 150°С, при участии серной кислоты , как водоотнимающего реагента):
Б) Отщепление галогенводородов при воздействии спиртового раствора щелочи:

Атом водорода отщепляется преимущественно от того атома углерода, который связан с меньшим числом атомов водорода (наименее гидрогенизированного атома) - правило Зайцева .
В) Дегалогенирование:

Химические свойства алкенов.
Свойства алкенов обуславливаются наличием кратной связи, поэтому алкены вступают в реакции электрофильного присоединения, которое протекает в несколько стадий (Н-Х - реагент):
1-я стадия:

2-я стадия:
 .
.
Ион водорода в такого типа реакциях принадлежит тому атому углерода, который имеет более отрицательный заряд. Распределение плотности такое:

Если в качестве заместителя стоит донор, который проявляется +I- эффект, то электронная плотность смещается в сторону наиболее гидрогенизированного атома углерода, создавая на нем частично отрицательный заряд. Реакции идут по правилу Марковникова : при присоединении полярных молекул типа НХ (HCl , HCN , HOH и т.д.) к несимметричным алкенам водород присоединяется преимущественно к более гидрогенизированому атому углерода при двойной связи.
А) Реакции присоединения:
1) Гидрогалогенирование:
Реакция идет по правилу Марковникова. Но если в реакции присутствует пероксид , то правило не учитывается:
2) Гидратация. Реакция идет по правилу Марковникова в присутствие фосфорной или серной кислоты :

3) Галогенирование. В результате происходит обесцвечивание бромной воды - это качественная реакция на кратную связь:
4) Гидрирование. Реакция протекает в присутствие катализаторов.
Алкены химически активны. Их химические свойства во многом определяются наличием двойной связи. Для алкенов наиболее характерны реакции электрофильного присоединения и реакции радикального присоединения. Реакции нуклеофильного присоединения обычно требуют наличие сильного нуклеофила и для алкенов не типичны. Алкены легко вступают в реакции окисления, присоединения а также способны к алильному радикальному замещению.
Реакции присоединения
Гидрирование Присоединение водорода (реакция гидрирования) к алкенам проводят в присутствии катализаторов. Чаще всего используют измельченные металлы - платину, никель, палладий и др. В результате образуются соответствующие алканы (насыщенные углеводороды).
$CH_2=CH_2 + H2 → CH_3–CH_3$
Присоединение галогенов. Алкены легко при обычных условиях вступают в реакции с хлором и бромом с образованием соответствующих дигалогеналканов, в которых атомы галогена находятся у соседних атомов углерода.
Замечание 1
При взаимодействии алкенов с бромом наблюдается обесцвечивание желто-бурой окраски брома. Это одна из старейших и самых простых качественных реакций на ненасыщенные углеводороды, поскольку аналогично реагируют также алкины и алкадиены.
$CH_2=CH_2 + Br_2 → CH_2Br–CH_2Br$
Присоединение галогеноводородов. При взаимодействии этиленовых углеводородов с галогеноводородами ($HCl$, $HBr$) образуются галогеналканы, направление реакции зависит от строения алкенов.
В случае этилена или симметричных алкенов реакция присоединения происходит однозначно и ведет к образованию только одного продукта:
$CH_2=CH_2 + HBr → CH_3–CH_2Br$
В случае несимметричных алкенов возможно образование двух разных продукта реакции присоединения:
Замечание 2
На самом деле в основном образуется только один продукт реакции. Закономерность направлении прохождения таких реакций установил российский химик В.В. Марковников в 1869 Она носит название правило Марковникова. При взаимодействии галогеноводородов с несимметричными алкенами атом водорода присоединяется по месту разрыва двойной связи в наиболее гидрированного атома углерода, то есть до того, что соединен с большим количеством атомов водорода.
Данное правило Марковников сформулировал на основе экспериментальных данных и только значительно позже оно получило теоретическое обоснование. Рассмотрим реакцию пропилена с хлористым водородом.
Одной из особенностей $p$-связи является его способность легко поляризоваться. Под влиянием метильной группы (положительный индуктивный эффект + $I$) в молекуле пропена электронная плотность $p$-связи смещается к одному из атомов углерода (= $CH_2$). Вследствие этого на нем возникает частичный отрицательный заряд ($\delta -$). На другом атоме углерода двойной связи в соответствии возникает частичный положительный заряд ($\delta +$).
Такое распределение электронной плотности в молекуле пропилена определяет место будущей атаки протоном. Это - атом углерода метиленовой группы (= $CH_2$), который несет частичный отрицательный заряд $\delta-$. А хлор, соответственно, атакует атом углерода с частичным положительным зарядом $\delta+$.
Как следствие, основным продуктом реакции пропилена с хлористым водородом является 2-хлорпропан.
Гидратация
Гидратация алкенов происходит в присутствии минеральных кислот и подчиняется правилу Марковникова. Продуктами реакции являются спирты
$CH_2=CH_2 + H_2O → CH_3–CH_2–OH$
Алкилирование
Присоединение алканов к алкенам в присутствии кислотного катализатора ($HF$ или $H_2SO_4$) при низких температурах приводит к образованию углеводородов с большей молекулярной массой и часто используется в промышленности для получения моторного топлива
$R–CH_2=CH_2 + R’–H → R–CH_2–CH_2–R’$
Реакции окисления
Окисление алкенов может происходить в зависимости от условий и видов окислительных реагентов как с разрывом двойной связи, так и с сохранением углеродного скелета:
Реакции полимеризации
Молекулы алкенов способны присоединяться при определенных условиях друг к другу с раскрытием $\pi$-связей и образования димеров, триммеров или высокомолекулярных соединений - полимеров. Полимеризация алкенов может протекать как по свободнорадикальному, так и катионно-анионому механизму. Как инициаторы полимеризации применяют кислоты, перекиси, металлы и др. Реакцию полимеризации осуществляют также под действием температуры, облучения, давления. Типичным примером является полимеризация этилена с образованием полиэтилена
$nCH_2=CH_2 → (–CH_2–CH_{2^–})_n$
Реакции замещения
Реакции замещения для алкенов не являются характерными. Однако при высоких температурах (свыше 400 ° C) реакции радикального присоединения, что носят обратимый характер, и подавляются. В этом случае становится возможным провести замещение атома водорода, находящегося в аллильном положении при сохранении двойной связи
$CH_2=CH–CH_3 + Cl_2 – CH_2=CH–CH_2Cl + HCl$
Алкены - более активный класс веществ, чем алканы. Химические свойства алкенов обусловлены строением их молекул.
Строение
Непредельные углеводороды - алкены или олефины - отличаются от других классов органических веществ наличием двойной или π-связи между атомами углерода. Двойная связь может находиться в любом месте молекулы.
Пи-связь образуется перекрыванием р-орбиталей. За счёт того, что р-орбиталь имеет расширения в обе стороны от оси и напоминает гантель, пи-связь возникает в двух местах. В отличие от σ-связи, возникающей при перекрывании s-орбиталей в виде сферы, π-связь менее прочная и легко разрушается под действием других соединений. Это обуславливает активность алкенов.

Рис. 1. π-связь и σ-связь.
Двойная связь в реакциях присоединения выступает в роли донора электронов. Поэтому алкенам свойственны реакции электрофильного присоединения.
Физические свойства
Общие физические свойства алкенов:
- температура плавления и кипения повышается с увеличением молекулярной массы в гомологическом ряду;
- не растворяются в воде;
- держатся на водной поверхности, так как имеют плотность во много раз меньше плотности воды;
- растворяются в органических растворителях - спиртах, эфирах.
Агрегатное состояние веществ меняется от количества атомов углерода в гомологическом ряду. Алкены с 2-4 атомами углерода - газы. От пептена (C 5 H 10) до гептадецена (C 17 H3 4) вещества находятся в жидком состоянии. Алкены, содержащие более 17 атомов углерода, являются твёрдыми телами.

Рис. 2. Гомологический ряд алкенов.
Химические свойства
Особенности и примеры химических свойств алкенов приведены в таблице.
|
Реакция |
Описание |
Уравнения реакций |
|
Гидрирование - присоединение водорода |
Протекает при высоком давлении в присутствии катализатора - никеля, палладия или платины. Образуются алканы - предельные углеводороды |
CH 2 =CH-CH 3 + H 2 → CH 3 -CH 2 -CH 3 |
|
Галогенирование - присоединение галогенов |
Протекает при обычных условиях. Галогены присоединяются по двойной связи. Образуются дигалогеналканы |
CH 2 =CH 2 + Cl 2 → Cl-CH 2 -CH 2 -Cl (1,2-дихлорэтан); CH 3 -CH=CH-CH 3 + Br 2 → CH 3 -CH-Br-CH-Br-CH 3 (2,3-дибромбутан) |
|
Гидрогалогенирование - присоединение галогеноводородов |
Реакция электрофильного присоединения. Электрофилом является протон водорода в составе галогена. Образуются галогеналканы |
CH 2 =CH 2 + HCl → CH 3 -CH 2 -Cl (хлорэтан) |
|
Гидратация - присоединение воды |
Реакция протекает в присутствии неорганических кислот - серной, фосфорной. Выполняют функцию катализатора и являются источниками водорода. Образуются одноатомные спирты |
CH 2 =CH 2 + H 2 O → CH 3 -CH 2 OH |
|
Полимеризация - увеличение числа атомов |
Протекает в присутствии катализатора, при повышенных давлении и температуре. Таким способом получают полиэтилен, поливинилхлорид, полипропилен |
nCH 2 =CH 2 → (-CH 2 -CH 2 -)n |
|
Протекает при избытке кислорода |
CH 2 =CH 2 + 3O 2 → 2CO 2 + H 2 O |
|
|
Неполное окисление |
Протекает в присутствии катализатора. Алкен, смешанный с кислородом, пропускают над нагретым серебром. Образуется эпоксид - оксид алкена |
2CH 2 =CH 2 + O 2 → 2CH 2 -O-CH 2 |
|
Реакция Вагнера |
Окисление перманганатом калия в щелочной или нейтральной среде. Образуются спирты |
3CH 2 =CH 2 + 2KMnO 4 + 4H 2 O → 3CH 2 OH-CH 2 OH + 2KOH + 2MnO 2 |
|
Окисление кипящим перманганатом калия в кислой среде |
Образуются карбоновые кислоты |
CH 3 -CH=CH-CH 3 + 4[O] → 2CH 3 COOH |
При нагревании в присутствии катализатора алкены вступают в реакцию изомеризации. Меняется положение двойной связи или структура углеродного скелета. Например, бутен-1 (положение двойной связи между первым и вторым атомами) превращается в бутен-2 (двойная связь «сдвигается» на второй атом).

Рис. 3. Изомеризация алкенов.
Что мы узнали?
Из урока химии 10 класса узнали о химических свойствах алкенов. Двойная связь делает эти вещества более активными, чем алканы. Алкены взаимодействуют с галогенами, кислородом, водой, водородом, галогеноводородами. Большинство реакций протекает в присутствии катализатора при высокой температуре или при повышенном давлении. Из алкенов получаются полимеры. Также под действием катализаторов образуются изомеры.
Тест по теме
Оценка доклада
Средняя оценка: 4.6 . Всего получено оценок: 64.
